Rezonansinių struktūrų braižymas
Originalus straipsnis: https://www.uky.edu/~rbgros1/CHE230/handouts/drawResonance.html
Autorius: Robert B. Grossman
Rezonansinės struktūros braižymas:
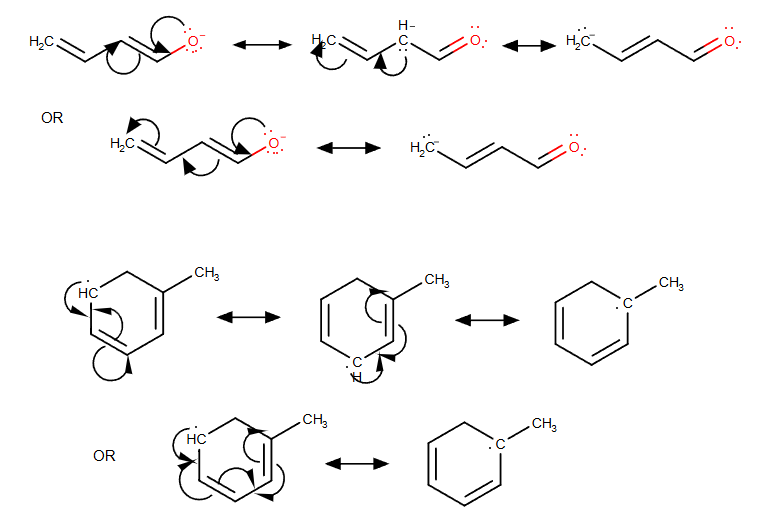
Ar yra žiedas (paprastai šešiakampis) su pakaitomis išsidėsčiusiomis dvigubomis jungtimis? Jei taip, perkelkite dvigubas jungtis ratu taip, kad jos būtų išsidėsčiusios pakaitomis.
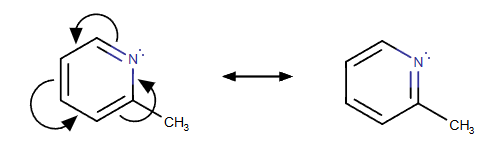
Ieškokite Ẍ−Y=Z, Ẍ−Y≡Z arba Ẍ=Y=Z. (X, Y ir Z gali turėti bet kokį formalųjį krūvį.) Tokiais atvejais perkelkite X atomo laisvąją elektronų porą, kad tarp X ir Y susidarytų papildoma π jungtis, o vieną iš π jungčių tarp Y ir Z nutraukite ir paverskite ją nauja laisvąja elektronų pora ant Z. X atomo formalusis krūvis padidėja 1, o Z atomo formalusis krūvis sumažėja 1.
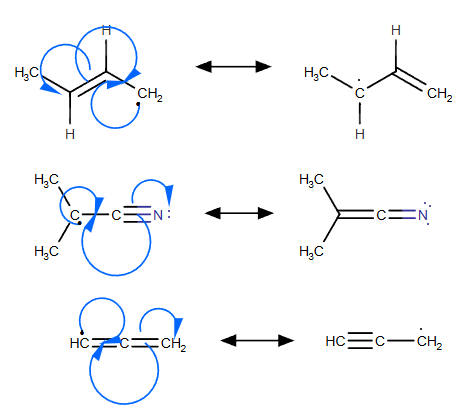
Ieškokite Ẋ−Y=Z, Ẋ−Y≡Z arba Ẋ=Y=Z. Tokiais atvejais naudokite vienakrypčią arba „žvejybos kabliuko“ formos elektronų srauto rodyklę, kad pavaizduotumėte pavienių elektronų judėjimą. Pastumkite nesidalijamą elektroną ant X, kad susidarytų papildoma π jungtis tarp X ir Y, paimkite vieną elektroną iš π jungties tarp Y ir Z ir panaudokite jį, kad užbaigtumėte papildomą π jungtį tarp X ir Y, o kitą elektroną paimkite iš π jungties tarp Y ir Z ir paverskite jį nauju nesidalijamu elektronu ant Z. Formaliosios krūvio vertės nesikeičia.
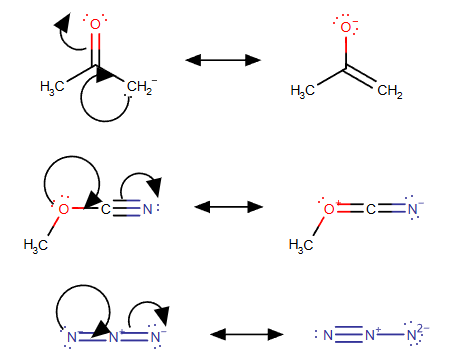
Ieškokite formulių +C−Y=Z, +C−Y≡Z arba +C=Y=Z. Šiais atvejais C atomas yra elektronų trūkumo būsenoje, turėdamas tik šešių elektronų sekstetą. (Kiti elektronų trūkumo turintys atomai, tokie kaip neutralus, trivalentis B, gali pakeisti C+, tačiau C+ yra žymiai dažniausias atvejis.) Naudokite elektronus iš vienos iš π ryšių tarp Y ir Z, kad sudarytumėte papildomą π ryšį tarp Y ir X. C+ įgyja oktetą ir tampa be krūvio; Z atomas tampa elektronų trūkumo turintis ir padidina savo formalųjį krūvį 1.
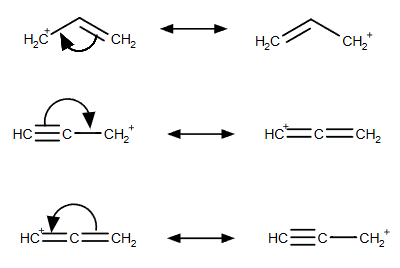
π ryšio (antrasis arba trečiasis ryšys tarp dviejų atomų) elektronai gali būti paskirstyti tarp dviejų atomų, sudarančių tą ryšį: du elektronai gali atitekti vienam atomui arba po vieną elektroną – kiekvienam atomui. Tokios rūšies rezonansas visada sukuria blogesnę (didesnės energijos) rezonansinę struktūrą, nes rezonansinėje struktūroje yra daugiau elektronų trūkumo turinčių atomų nei pradinėje struktūroje. Jei vienam atomui skiriate du elektronus, to atomo formalusis krūvis sumažėja 1, o kito atomo formalusis krūvis padidėja 1.
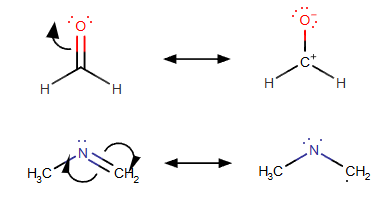
Jei turite keletą greta esančių π ryšių, elektronus galite perkelti keletą pozicijų žemyn grandine.